Boiler combustion part III
Phase of combustion in solid fuel VS Heat of combustion in Boiler
Phase of combustion in solid fuel
พิจารณาการเผาไหม้ของเชื้อเพลิงแข็ง หน้าที่หลักของห้องเผาไหม้ (ใน boiler) คือ การควบคุมองค์ประกอบหลัก ของการเผาไหม้ที่เกิดขึ้นให้เหมาะสม โดยมีปัจจัยหลักๆ ที่สำคัญอยู่ด้วยกัน 2 อย่างคือ
1. ปริมาณเชื้อเพลิง ต่อหน่วยเวลา(fuel rate) ที่ป้อนเข้าสู่ห้องเผาไหม้ โดยนับตั้งแต่ เกิดการเริ่มการเผาไหม้ จนกระทั่ง การเผาไหม้สิ้นสุด(burnt out) ต้องใช้เวลาที่เพียงพอ และเหมาะสม
2. ปริมาณอากาศ(air rate) ต่อหน่วยเวลา ที่ป้อนเข้าสู่ห้องเผาไหม้ โดยที่มีปริมาณเหมาะสมในการคลุกเคล้า กับปริมาณเชื้อเพลิง
การเผาไหม้ของเชื้อเพลิงแข็ง (ผู้เขียนจะ ยกตัวอย่างไปที่ถ่านหิน เป็นหลัก เพื่อให้เห็นภาพง่ายที่สุดก่อน) โดยขอให้พวกเราจินตนาการภาพตามกันไป เมื่อเชื้อเพลิงแข็ง(ถ่านหิน)ของพวกเรา กำลังเดินทางเข้าสู่ห้องเผาไหม้ เพื่อเตรียมตัวเผาไหม้ ยกตัวอย่างเป็น travelling grate-เพื่อให้จินตนาการ ให้ง่ายต่อความเข้าใจนะครับ(ทั้งนี้ และทั้งนั้น ในห้องเผาไหม้ประเภทอื่นๆ เช่นพวก Dumping grate หรืออย่าง pushing/step grate แม้แต่ fixed grate ก็ใช้หลักการเดียวกัน/หรือ ลำดับการเผาไหม้ จะประมาณเดียวกัน) โดยเบสิคที่พวกเราต้องทำความเข้าใจ จะมาจากตรงนี้ก่อน เบสิคแน่นแล้วเราค่อยไป advances กันครับ จะพิสดารขนาดไหน ก็ล้วนเริ่มต้นจากหลักการเดียวกัน
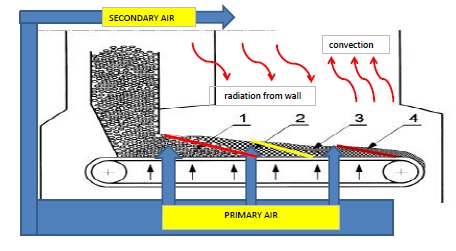
โดยในภาคทฤษฎีของการ burn หรือการเผาไหม้ ของถ่านหินที่เราสนใจนั้น จะมี step หรือ ลำดับขั้นในการ burn อยู่ 3 step (ภาษาอังกฤษ เพื่อนชาวอเมริกันของนายช่าง มักนิยมเรียกว่า 3 steps of mass loss) ดังนี้-ถ่านหิน กำลังวิ่งเข้าสู่ห้องเผาไหม้แล้วครับ พวกเรานึกภาพตามผมไปได้เลย พร้อมภาพประกอบ นั่นคือ หมายเลข 1,2 และ 3 ตามลูกศรชี้(ส่วนหมายเลข 4 นั่นเป็นส่วนของ ขี้เถ้า/Ash อย่าเพิ่งไปสนใจมัน) นั่นคือ ลำดับการ burn ดังต่อไปนี้
พิจารณาการเผาไหม้ของเชื้อเพลิงแข็ง หน้าที่หลักของห้องเผาไหม้ (ใน boiler) คือ การควบคุมองค์ประกอบหลัก ของการเผาไหม้ที่เกิดขึ้นให้เหมาะสม โดยมีปัจจัยหลักๆ ที่สำคัญอยู่ด้วยกัน 2 อย่างคือ
1. ปริมาณเชื้อเพลิง ต่อหน่วยเวลา(fuel rate) ที่ป้อนเข้าสู่ห้องเผาไหม้ โดยนับตั้งแต่ เกิดการเริ่มการเผาไหม้ จนกระทั่ง การเผาไหม้สิ้นสุด(burnt out) ต้องใช้เวลาที่เพียงพอ และเหมาะสม
2. ปริมาณอากาศ(air rate) ต่อหน่วยเวลา ที่ป้อนเข้าสู่ห้องเผาไหม้ โดยที่มีปริมาณเหมาะสมในการคลุกเคล้า กับปริมาณเชื้อเพลิง
การเผาไหม้ของเชื้อเพลิงแข็ง (ผู้เขียนจะ ยกตัวอย่างไปที่ถ่านหิน เป็นหลัก เพื่อให้เห็นภาพง่ายที่สุดก่อน) โดยขอให้พวกเราจินตนาการภาพตามกันไป เมื่อเชื้อเพลิงแข็ง(ถ่านหิน)ของพวกเรา กำลังเดินทางเข้าสู่ห้องเผาไหม้ เพื่อเตรียมตัวเผาไหม้ ยกตัวอย่างเป็น travelling grate-เพื่อให้จินตนาการ ให้ง่ายต่อความเข้าใจนะครับ(ทั้งนี้ และทั้งนั้น ในห้องเผาไหม้ประเภทอื่นๆ เช่นพวก Dumping grate หรืออย่าง pushing/step grate แม้แต่ fixed grate ก็ใช้หลักการเดียวกัน/หรือ ลำดับการเผาไหม้ จะประมาณเดียวกัน) โดยเบสิคที่พวกเราต้องทำความเข้าใจ จะมาจากตรงนี้ก่อน เบสิคแน่นแล้วเราค่อยไป advances กันครับ จะพิสดารขนาดไหน ก็ล้วนเริ่มต้นจากหลักการเดียวกัน
โดยในภาคทฤษฎีของการ burn หรือการเผาไหม้ ของถ่านหินที่เราสนใจนั้น จะมี step หรือ ลำดับขั้นในการ burn อยู่ 3 step (ภาษาอังกฤษ เพื่อนชาวอเมริกันของนายช่าง มักนิยมเรียกว่า 3 steps of mass loss) ดังนี้-ถ่านหิน กำลังวิ่งเข้าสู่ห้องเผาไหม้แล้วครับ พวกเรานึกภาพตามผมไปได้เลย พร้อมภาพประกอบ นั่นคือ หมายเลข 1,2 และ 3 ตามลูกศรชี้(ส่วนหมายเลข 4 นั่นเป็นส่วนของ ขี้เถ้า/Ash อย่าเพิ่งไปสนใจมัน) นั่นคือ ลำดับการ burn ดังต่อไปนี้
|
คลิกที่รูป เพื่อขยาย
- ถ่านหินไหลลงมา เข้าห้องเผาไหม้ วิ่งบน travelling grate จาก ซ้ายมือ --> ขวามือ รูปที่ 1. เป็น basic ที่จะอธิบาย หลักการ burn ใน เชื้อเพลิงแข็งได้เป็นอย่างดี ลูกศร No.1, 2, 3 และ 4 คือ เรื่องที่เราจะคุยกันใน episode นี้
|
รูป 2. เอารูปที่ 1 มาแปลงร่าง เป็นของจริงกัน หน้าตาก็จะออกมา ประมาณนี้ครับ
|
ลำดับที่ 1 คือ Drying (ลูกศร หมายเลข 1)
อธิบายโดยย่อ คือ Drying process (ลูกศร หมายเลข 1. ตามภาพประกอบ) จะเป็นกระบวนการทางความร้อนที่มาจาก convection+radiation ในตัวห้องเผาไหม้ ผ่านมาที่ surface ของตัวเชื้อเพลิง หลังจากนั้นจะเป็น conduction ในตัวเชื้อเพลิง โดยวัตถุประสงค์หลัก Drying คือการทำให้แห้ง หรือ ทำให้โมเลกุลของน้ำ(ความชื้น)-ทั้งความชื้นที่ผิวหน้า/ความชื้นด้านในตัวเชื้อเพลิง หายไป ทำให้มันออกไป ทำให้มันระเหยออกไป หรือว่า vaporize ไปเสียนั่นเอง เนื่องจากเราไม่ต้องการใน combustion ของพวกเรา ถูกต้องหรือไม่ครับ ดังนั้นใน step นี้ พิจารณา size หรือ ขนาดของเชื้อเพลิงแข็ง(ถ่านหิน) ที่วิ่งเข้าห้องเผาไหม้ size เล็ก ย่อมใช้ drying time น้อยกว่า ขนาด size ใหญ่ ถูกต้องหรือไม่(sizing ของเชื้อเพลิงแข็ง ค่อนข้างจะมีผลเยอะ-ขอกล่าวในลำดับถัดไป) ดังนั้น drying process ในลำดับนี้ มันคือ การ warming (หรือ absorbed heat) นั่นเอง โดย อุณหภูมิจะอยู่ที่ประมาณ 100 องศาเซลเซียส บวก ลบ โดยประมาณ
ลำดับที่ 2 คือ Devolatilization
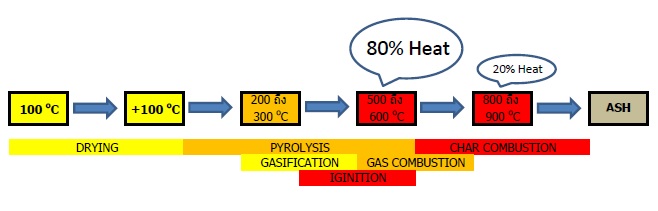
หลังจากที่เชื้อเพลิงของพวกเรา ได้รับความร้อน(ที่มาจากส่วนแรก คือ drying) มาเป็นจำนวน ช่วงเวลาหนึ่งแล้วนั้น ความร้อนที่สะสมในตัวเชื้อเพลิง ก็จะเพิ่มขึ้น จนกระทั่งถึงลำดับที่ 2 ของการเผาไหม้ กล่าวคือ Devolatilization หรือในบางตำรา เราจะเรียกว่า pyrolysis กล่าวคือ ณ ตำแหน่งนี้ จะเป็นจุดเริ่มต้นของการเผาไหม้ โดยที่จะเกิดการแตกตัวออก ของelement ในเชื้อเพลิงแข็ง พวกที่ให้ความร้อนออกมา พร้อมกับสถานะที่เป็นก๊าซ/gasification หรือกล่าวให้ง่ายคือ พวกสารระเหย (Volatile matter) ที่เป็นตัวกลาง ก่อนที่จะเริ่มการเผาไหม้ จะถูกแตกตัวออกมาใน Devolization process นี้ (ประมาณ 300-400 องศาเซลเซียส จะเริ่มแล้ว)
Pyrolysis และเมื่อได้รับความร้อนไปเรื่อยๆ การเผาไหม้ของพวก volatile ก็จะเริ่มติดไฟ (ประมาณ 400-600 องศาเซลเซียส-ตรงนี้ ติดไฟแล้วนะ ignition แล้ว ว่าง่ายๆ นั่นคือ gas combustion จะเกิดขึ้นตรงจุดนี้ กว่า80% ของความร้อน จะมากจากตรงนี้) โดย CO, CO2 และก๊าซ ที่เป็นผลมาจากการเผาไหม้ของพวก hydrocarbon รวมถึง hydrogen จะออกมาในช่วงอุณหภูมิ 700-900 องศาเซลเซียส โดยจะสิ้นสุดกระบวนการ pyrolysis ที่อุณหภูมิประมาณ 900 องศาเซลเซียส (โดยถัดจาก อุณหภูมินี้ไป ในการเผาไหม้ที่เหลืออยู่ นั่นคือ fix carbon หรือ char และขี้เถ้า คือองค์ประกอบหลักที่เหลืออยู่นั่นเอง)
ดังนั้นพวกเราจะเห็นว่า หากเชื้อเพลิงของเรา มีปริมาณ Volatile ที่มีปริมาณมาก จะทำให้เกิดการลุกติดไฟได้ง่าย และรวดเร็ว(สาเหตุ มันมาจาก ignition temp มันจะต่ำกว่า) และในทำนองกลับกัน หากเชื้อเพลิงของเรา มีปริมาณ Volatile ต่ำ ก็จะเกิดการติดไฟยาก และการลุกไหม้อย่าง ช้า ๆนั่นเอง ครับ
ลำดับที่ 3 คือ Char combustion
กลับไปดูที่รูปเราเหมือนเดิม ในลูกศร หมายเลข 3. พิจารณาตามลำดับการเผาไหม้ Char combustion จะเป็นการเผาไหม้ ที่ใช้เวลา ที่มากที่สุดกล่าวคือ การเผาไหม้ในช่วงนี้จะเป็นการเผาไหม้ในส่วนของelement หรือส่วนขององค์ประกอบ ที่ติดไฟ(ยาก) ดังนั้นในบางครั้งเราจึงพบเห็น องค์ประกอบหลายๆส่วน(ที่มันติดไฟยาก ที่มันเผาไหม้ยาก)นี้ ออกมาพร้อมกับขี้เถ้า ในสภาวะที่เกิดการลุกไหม้แต่ยังไม่หมด(ส่วนนี้นั่นเอง ที่เราเรียกมันว่า char combustion) รวมไปถึง ส่วนที่มันยังไม่ลุกไหม้ และออกมา(เพราะมันติดไฟยาก และ/หรือ ใช้เวลาในการลุกไหม้, ติดไฟนาน นั่นเอง-คือ มันใช้เวลานาน กว่ามันจะไหม้ ยิ่งไปเทียบเวลากับ Devolatilization step แล้ว คนละเรื่องเลย) นี่คือ Char combustion
ดังนั้น หากเราพิจารณาการเผาไหม้ จาก step ที่ 2 คือ Devolatilization และ step ที่ 3 คือ Char combustion แล้วจะพบว่า main process หรือ reaction type ในส่วนของปฏิกิริยาการ burn นั้น พวกเรา สามารถกล่าวได้ว่า
Volatiles หรือ พวกสารวาบไฟ/gasification จะเป็นการเผาไหม้แบบ homogenous (กล่าวคือ เชื้อเพลิง,ตัวตั้งต้นที่ทำปฏิกิริยา + ตัว oxidizer,อากาศ อยู่ในสถานะเดียวกัน(สถานะก๊าซ) เราจึงเรียกมันว่า homogenous)
และในทำนองเดียวกัน ส่วน Char combustion จะกล่าวได้ว่าเป็น heterogenous combustion (กล่าวคือ เชื้อเพลิง,ตัวที่ทำปฏิกิริยา + ตัว oxidizer,อากาศ อยู่ที่คนละสถานะ(ของแข็ง-ก๊าซ) เราจึงเรียกมันว่า heterogenous) ก็ไม่ผิดหลักการแต่อย่างไร ตรงนี้ พวกเราต้องเข้าใจก่อนนะครับ ก่อนที่จะไปใน episode ถัดไปที่ยากขึ้นไปกว่านี้ มันจะ link ไปสู่ กระบวนการทางความร้อนทางเคมี รวมไปถึง การออกแบบทางความร้อน(Thermal design) อีกด้วย ดังนั้นพวกเราจึงต้อง พูดจากันในภาษาเดียวกัน นั่นคือ ภาษา combustion นั่นเองครับ
คำถามชวนคิด
*** อ่านมาถึงตรงนี้ พวกเราอาจจะมีคำถาม แล้วเราจะทราบได้อย่างไร ว่า เชื้อเพลิงเรามี volatile สูง หรือ ต่ำ ? พวกเราพอจะพิจารณาคร่าวๆ ได้จากอะไรบ้างครับ ?
*** พวกเราลองคิดเล่นๆ ถ่านหินของผม เรียงลำดับตาม heating value โดยผมหยิบยกมา 3 ตัวพอครับ อันได้แก่ แอนทราไซต์, ไบทูบินัส และ ลิกไนต์ ตามลำดับ คำถามชวนคิด คือ ใน 3 ตัวนี้ พวกเราคิดว่า ตัวไหน จะมี fixed carbon เยอะที่สุด เพราะเหตุใด ?
*** อ่านมาถึงตรงนี้ พวกเราอาจจะมีคำถาม แล้วเราจะทราบได้อย่างไร ว่า เชื้อเพลิงเรามี volatile สูง หรือ ต่ำ ? พวกเราพอจะพิจารณาคร่าวๆ ได้จากอะไรบ้างครับ ?
*** พวกเราลองคิดเล่นๆ ถ่านหินของผม เรียงลำดับตาม heating value โดยผมหยิบยกมา 3 ตัวพอครับ อันได้แก่ แอนทราไซต์, ไบทูบินัส และ ลิกไนต์ ตามลำดับ คำถามชวนคิด คือ ใน 3 ตัวนี้ พวกเราคิดว่า ตัวไหน จะมี fixed carbon เยอะที่สุด เพราะเหตุใด ?
ปฏิกริยาที่เกิดขึ้น ในเชื้อเพลิงแบบต่างๆ
|
|
สถานะของเชื้อเพลิง
เชื้อเพลิงแข็ง เชื้อเพลิงเหลว เชื้อเพลิงก๊าซ |
HOMOGENOUS
สารวาบไฟ / Volatile เกิดขึ้นหลังจาก evaporation พวก base reaction |
HETEROGENOUS
Fixed carbon การเผาไหม้พวกเขม่า การเผาไหม้พวกเขม่า |
Heat of combustion in fuel
ตัดกลับมาที่ ความร้อนที่เกิดขึ้น จากการเผาไหม้ (ทั้งแบบ Homogenous และ Heterogeneous) จะพบว่า ความร้อนที่เราได้ออกมา จากปฏิกิริยาเคมี หรือ oxidation ที่เกิดขึ้น combustion process จะอยู่ในช่วงของ Pyrolysis 80% โดยประมาณ (มาจาก gas combustion) และ char combustion 20% โดยประมาณ(ใน solid fuel)
เรากำลังจะเกริ่นนำ เพื่อนำท่านเข้าสู่ อุณหพลศาสตร์ของการเผาไหม้(Thermodynamic of combustion) โดยในเบื้องต้น พิจารณา Oxidation reaction ที่เกิดขึ้น ในกรณีที่เกิดขึ้นของ เชื้อเพลิงแข็ง และเชื้อเพลิงเหลว ที่พวกเราคุ้นเคยกันใน ultimate analysis(กล่าวคือ จะว่ากันตามสัดส่วนโดยมวล ในส่วนขององค์ประกอบหลัก) ความเดิมจาก ภาคทฤษฎีการเผาไหม้ C, H และ S คือ พระเอก ดังนั้น นางเอกจะเป็นอะไรไปไม่ได้นอกจาก O2 ย้อนกลับไปที่ ultimate analysis ในตัวเนื้อของเชื้อเพลิง(แข็ง และ เชื้อเพลิงเหลว) ที่เกิดการเผาไหม้ สักครู่มันจะลิงค์กันเอง
เรากำลังจะเกริ่นนำ เพื่อนำท่านเข้าสู่ อุณหพลศาสตร์ของการเผาไหม้(Thermodynamic of combustion) โดยในเบื้องต้น พิจารณา Oxidation reaction ที่เกิดขึ้น ในกรณีที่เกิดขึ้นของ เชื้อเพลิงแข็ง และเชื้อเพลิงเหลว ที่พวกเราคุ้นเคยกันใน ultimate analysis(กล่าวคือ จะว่ากันตามสัดส่วนโดยมวล ในส่วนขององค์ประกอบหลัก) ความเดิมจาก ภาคทฤษฎีการเผาไหม้ C, H และ S คือ พระเอก ดังนั้น นางเอกจะเป็นอะไรไปไม่ได้นอกจาก O2 ย้อนกลับไปที่ ultimate analysis ในตัวเนื้อของเชื้อเพลิง(แข็ง และ เชื้อเพลิงเหลว) ที่เกิดการเผาไหม้ สักครู่มันจะลิงค์กันเอง
|
C + O2 = CO2 S + O2 = SO2 2H2 + O2 = 2H2O |
เมื่อเราพิจารณา 1 อะตอม ของ C ในปฏิกิริยา oxidation ที่เกิดขึ้น (หรือพูดให้ง่ายคือ เอา C 1 อะตอม ไปเผาไหม้) สิ่งที่เราได้ออกมา คือ ค่าของพลังงานความร้อนที่เกิดขึ้น โดยกรณีนี้ C นี้ คือ
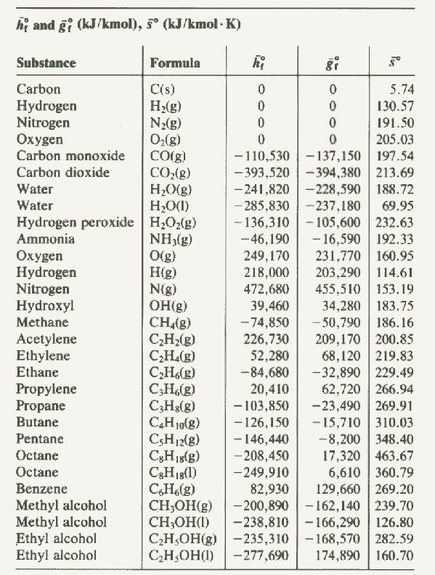
C(s) + O2(g) = CO2(g) Δh = - 393.5 kj/mol *จาก Enthalpy formation ที่มา: Thermodynamic |
-393.5 kj/mol ค่าพลังงานความร้อน ที่เกิดขึ้นจาก oxidation reaction นี้ คือ 393.5 kj/mol โดยที่ ติดลบ (-) คือ การคายความร้อน(ออกจากระบบ), จะเรียกว่า ปล่อยพลังงานออกมาก็ไม่ผิด หรือ enthalpy ที่เปลี่ยนแปลงไป มีค่า -393.5 kj/mol นั่นเอง(หรือ) ค่าความร้อน ที่มันเกิดขึ้น ต่อ 1 โมล ถ้าพวกเราไปอ่านตำราเพื่อนชาวอเมริกัน มักจะเรียกว่า Heat of formation ครับ มันคือพลังงานนะพวกเรา ในขณะนี้ เรากำลังพูดถึงพลังงาน ในสมการเคมีที่เกิดขึ้น พวกเราอย่าเพิ่งสับสน
|
Product ของเรา ที่กำลังพิจารณา ในตอนนี้คือ CO2(g) CO2 มาจากสารตั้งต้น C(s) + O2(g) ที่ผ่าน oxidation reaction ดังนั้น ค่าความร้อน(พลังงาน)ที่ถ่ายเท หรือ ที่เกิดขึ้น มันคือ Q = Δh = - 393.5 kj/mol = (hP - hR) หรือ enthalpy formation = heat formation ดังนั้น พวกเราจะเห็นว่า สิ่งที่เกิดขึ้นใน complete combustion หรือ ผลลัพธ์ของสมการ การเผาไหม้แบบสมบูรณ์ ของพวกเรา (ในทางทฤษฎี) คือ CO2(g) และ H2O(g) โดยที่ขณะนี้ เรายังไม่ต้องสนใจ ตัวตั้งต้นของสมการ(จะมาจากเชื้อเพลิงอะไรก็ได้ เชื้อเพลิงแข็ง เชื้อเพลิงเหลว หรือ แกสก็ได้) เมื่อมี complete combustion พวกเราจะได้ CO2(g) และ H2O(g) นี่คือ ทฤษฎี ถูกต้องนะครับ และในทางเดียวกัน formation ที่เกิดขึ้น H2O(g) พวกเราจะได้ Δh = - 241.8 kj/mol (จากตาราง) เช่นเดียวกัน ติดลบ(-) คือ ปฏิกิริยา คายความร้อนเหมือนกัน ย้อนกลับไปที่ ultimate analysis พวกเราร้องอ๋อ กันหรือยังครับ by mass ที่เป็นสัดส่วน C ที่มี by mass, H ที่มี by mass, S ที่มี by mass ในส่วนของเชื้อเพลิงแข็ง และ เชื้อเพลิงเหลว จับเข้าสมการการเผาไหม้ ให้ง่ายที่สุด ให้มันเป็น complete combustion ทำไม factor หลักของความร้อน Heating value อันเป็นหัวใจ ของความร้อนที่เราต้องการในการเผาไหม้ หรือ Heat of combustion ใน(แต่ละ)เชื้อเพลิงนั้นๆ จึงมาจาก C ในส่วนผสมหลัก (พิจารณา ค่า C ในถ่านหินแบบ ลิกไนต์/ ไบทูบินัส/ แอนทราไซต์ เทียบกับ Heating value สัดส่วนที่ได้) จึงเป็นผลลัพธ์ ให้เรามองในภาพรวมทั้งหมด คือ Heat of combustion โดยเฉพาะอย่างยิ่ง ในเชื้อเพลิงแข็ง และ เชื้อเพลิงเหลว ที่เป็น combustion by mass นั่นเอง |
เอามาจากไหน ?
คำตอบคือ หนังสือ Thermodynamics ที่พวกเราเรียนกัน |
Heat of combustion = Heat formation(ผลลัพธ์) – Heat formation(ตัวตั้งต้น)
โดยนี่คือทางทฤษฎี และ เชื้อเพลิงแกส หรือ gas fuel ก็เช่นกัน หากแต่เชื้อเพลิงแกส(สถานะ) เราจะคุยกันในภาษา ของ volumetric เป็นหลัก ในสัดส่วน mol ที่เกิดขึ้น หรือ ผู้เขียนขอเรียกว่า combustion by volume โดยเฉพาะอย่างยิ่งในพวก Hydrocarbon ที่พวกเรา พบเจอกันบ่อยๆ หรือนิยมเรียกว่าพวก CxHy เป็นหลัก หลักการเดียวกัน heat formation เหมือนกัน โดยพวกเราจะเห็นได้ว่า combustion equation ของพวก hydrocarbon นี้ ยิ่งเข้าสมการ ในทางทฤษฎี complete combustion ที่ค่อนข้างจะเป็นรูปแบบตายตัว
|
นั่นคือ CxHy + (x+0.25y)O2 = (x)CO2 + (0.5y)H2O
เพื่อให้มองภาพออก เบสิค 1 ตัวอย่าง มีเทน หรือ CH4 ง่ายที่สุดในโลกแล้ว ไม่มีอะไรง่ายไปกว่านี้แล้ว ความร้อนจากการเผาไหม้ มีเทน ที่เราพิจารณา หรือ Heat of combustion ของมีเทน เขียนสมการ การเผาไหม้(complete combustion)ก่อนครับพวกเรา จะได้ว่า CH4 (g) + 2 O2 (g) = CO2 (g) + 2 H2O (g) |
Heat of combustion = heat formation(ผลลัพธ์) – heat formation(ตัวตั้งต้น)
Heat of combustion = [heat formation of CO2 (g) + 2 x heat formation of H2O (g)] - [heat formation of CH4 (g) + 2 x heat formation of O2 (g)]
*จาก Enthalpy formation ที่มา: Thermodynamic
Heat of combustion = [ -393.5 kJ + 2x(-241.8 kJ)] - [-74.8 kJ + 2x(0 kJ)]
ความร้อนจากการเผาไหม้ มีเทน = - 802.3 kJ
ทีนี้ พวกเราหยิบเครื่องคิดเลข ตามมาแล้ว ลองจิ้มดู ความร้อนจากการเผาไหม้ ของ บิวเทน หรือ C4H10 แล้วลองเปรียบเทียบ ค่าที่เราได้เบื้องต้น จากมีเทน/ CH4 กันดูครับ
Heat of combustion = [heat formation of CO2 (g) + 2 x heat formation of H2O (g)] - [heat formation of CH4 (g) + 2 x heat formation of O2 (g)]
*จาก Enthalpy formation ที่มา: Thermodynamic
Heat of combustion = [ -393.5 kJ + 2x(-241.8 kJ)] - [-74.8 kJ + 2x(0 kJ)]
ความร้อนจากการเผาไหม้ มีเทน = - 802.3 kJ
ทีนี้ พวกเราหยิบเครื่องคิดเลข ตามมาแล้ว ลองจิ้มดู ความร้อนจากการเผาไหม้ ของ บิวเทน หรือ C4H10 แล้วลองเปรียบเทียบ ค่าที่เราได้เบื้องต้น จากมีเทน/ CH4 กันดูครับ
พอจับประเด็น พอจับไอเดีย ได้หรือไม่ครับพวกเรา สำหรับตอนนี้ Heat of combustion in Boiler มันมายังไง มันมาจากไหน factor หลัก, หัวใจหลักเรายังอยู่กันที่เชื้อเพลิงกันก่อนนั่นเอง เชื้อเพลิงแบบไหน? เชื้อเพลิงแข็ง, เหลว หรือ เชื้อเพลิงก๊าซ โดยที่ part นี้ ผู้เขียนน่าจะเรียกได้ว่า ทบทวน Thermodynamics กันอีกสักรอบ โดยอันที่จริงแล้ว มันสัมพันธ์กันนั่นเอง Thermodynamic + Combustion + Heat transfer = Boiler 1 ลูก โดยที่เราจะเริ่มต้นจาก Combustion equation นั่นเอง โดยพวกเรา อย่าลืมสิ่งที่ผู้เขียนเน้นย้ำอยู่เสมอ สำหรับ สมการการเผาไหม้ มันออกได้ไม่กี่หน้านั่นเอง ดังนั้น ตรงนี้ ต้องขึ้นใจแล้วนะครับพวกเรา เพราะ part ต่อไป จะ advance กว่านี้นั่นเอง
|
Complete combustion
เชื้อเพลิง + Oxygen = CO2 + H2O Incomplete combustion เชื้อเพลิง + Oxygen = C + H2O หรือ (เขม่า + H2O) เชื้อเพลิง + Oxygen = CO + H2O หรือ (คาร์บอนมอนนอกไซด์ + H2O) เชื้อเพลิง + Oxygen = CO + C + H2O หรือ (คาร์บอนมอนนอกไซด์ + เขม่า +H2O) |
ณัฐพงศ์ ไชยสิทธิ์ วก.958 วุฒิวิศวกรเครื่องกล |